11 月 30 日,國家藥監局藥品審評中心(CDE)官網最新公示,上海科濟制藥的 CT053 全人抗 BCMA 自體 CAR-T 細胞注射液擬納入突破性療法,用于治療復發難治多發性骨髓瘤。
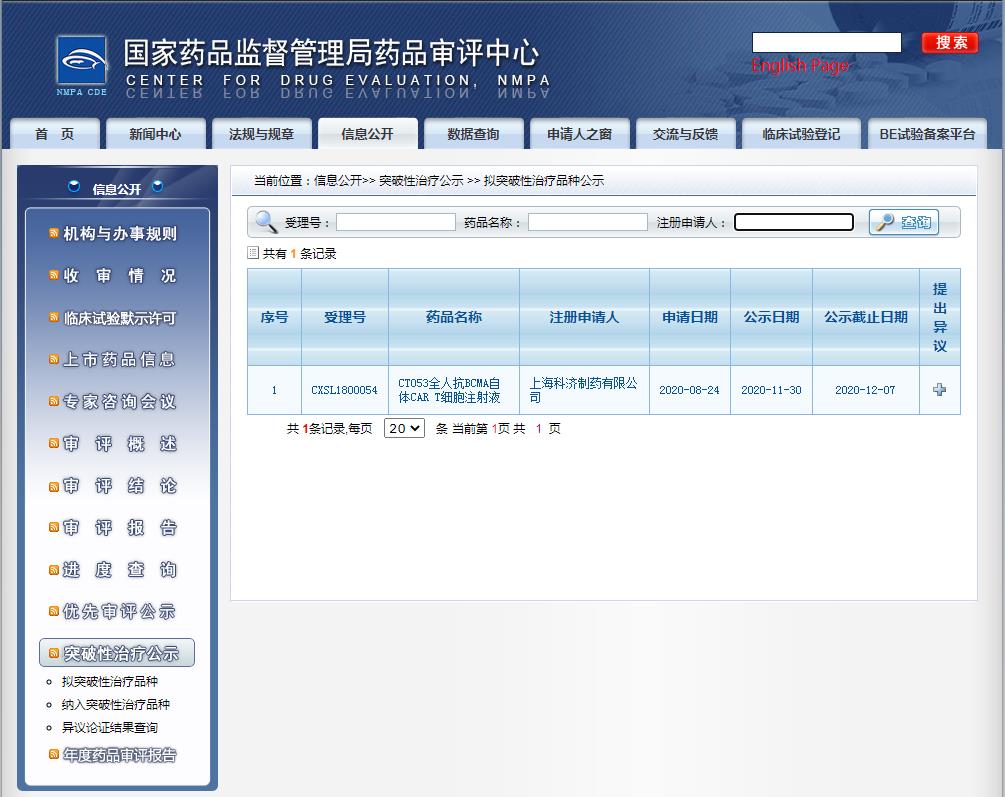
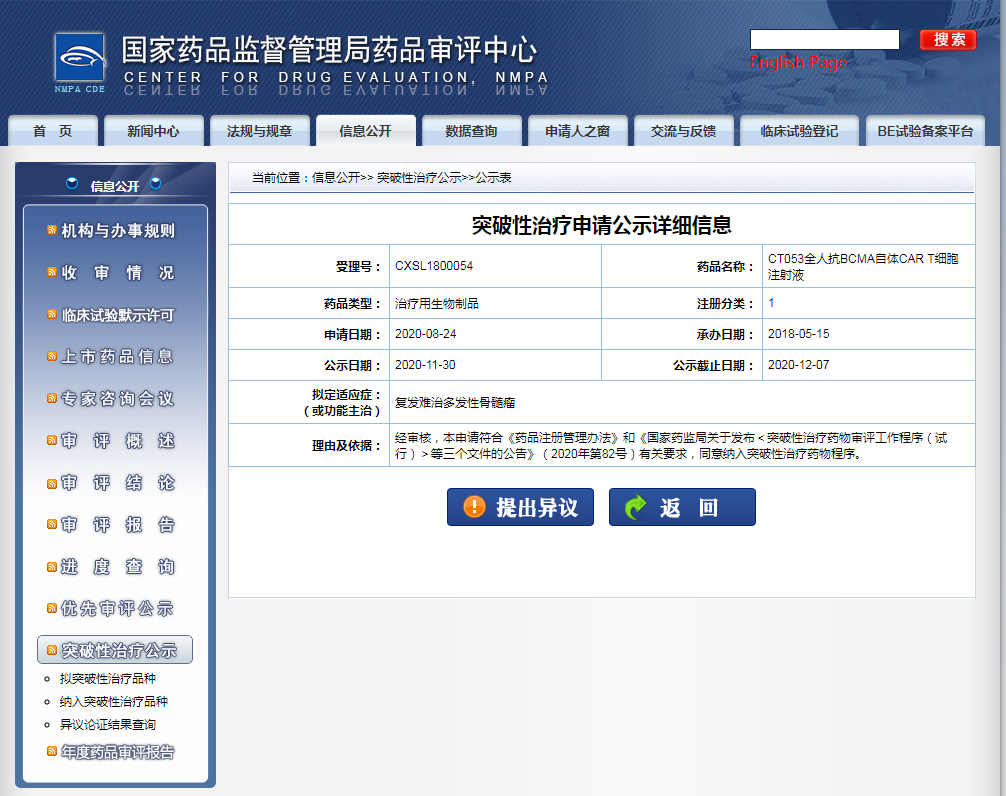
截圖來源:CDE官網
這是第 3 個擬納入突破性療法的 CAR-T 產品,與此前納入突破性療法的傳奇生物 LCAR-B38M 同樣靶向 BCMA。

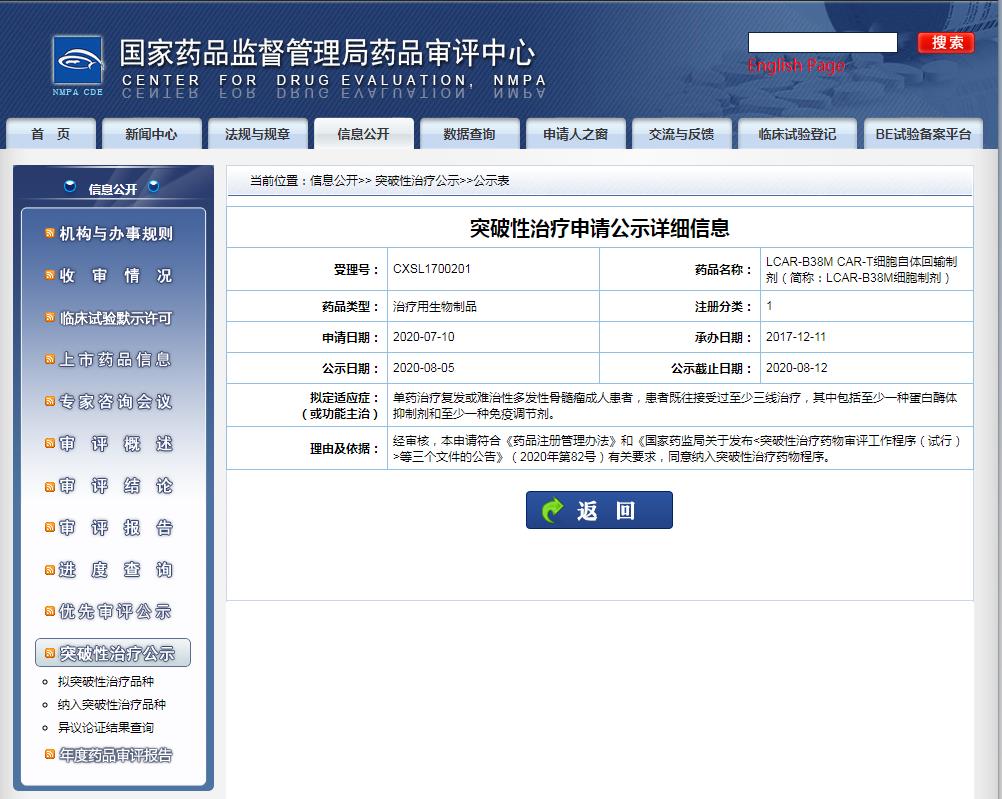
截圖來源:CDE官網
CT053 是科濟生物開發的全人抗 BCMA 的 CAR-T 細胞產品,用于復發難治多發性骨髓瘤。目前,該藥在國內正處于 I/II 期臨床階段(CTR20190955)。
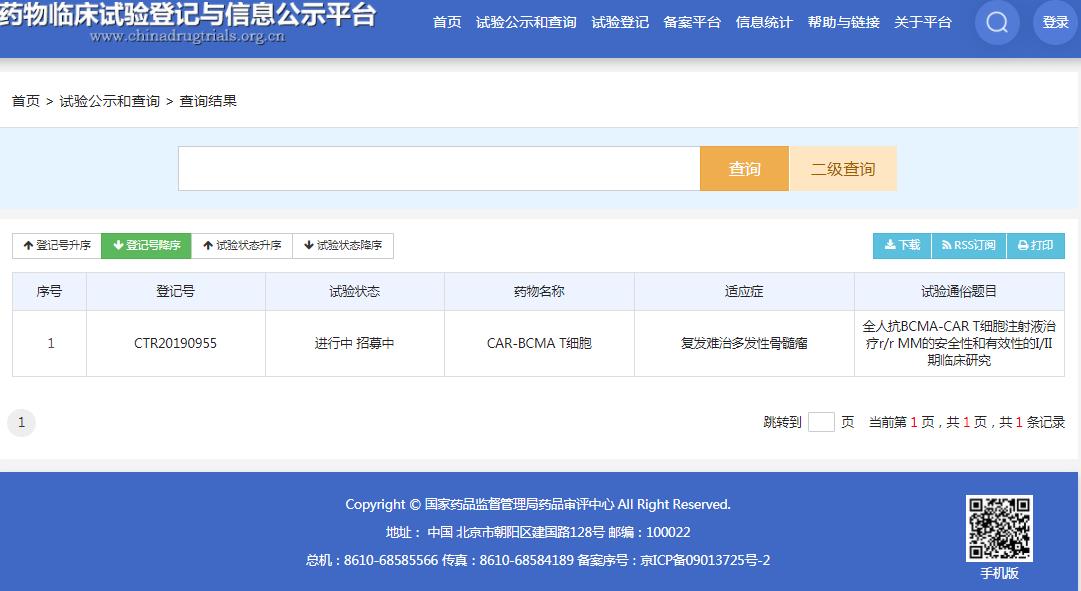
截圖來源:CDE官網
多發性骨髓瘤是一種克隆性漿細胞異常增殖的惡性疾病,復發/難治多發性骨髓瘤(R/R MM)有重大的未滿足的醫學需求。B 細胞成熟抗原(BCMA)靶向的嵌合抗原受體(CAR)基因工程修飾的 T 細胞,被認為是一種治療多發性骨髓瘤的新手段。本次科濟的 CT053 擬納入突破性療法,將獲得CDE 更多的臨床指導和溝通交流機會,加速其臨床開發。
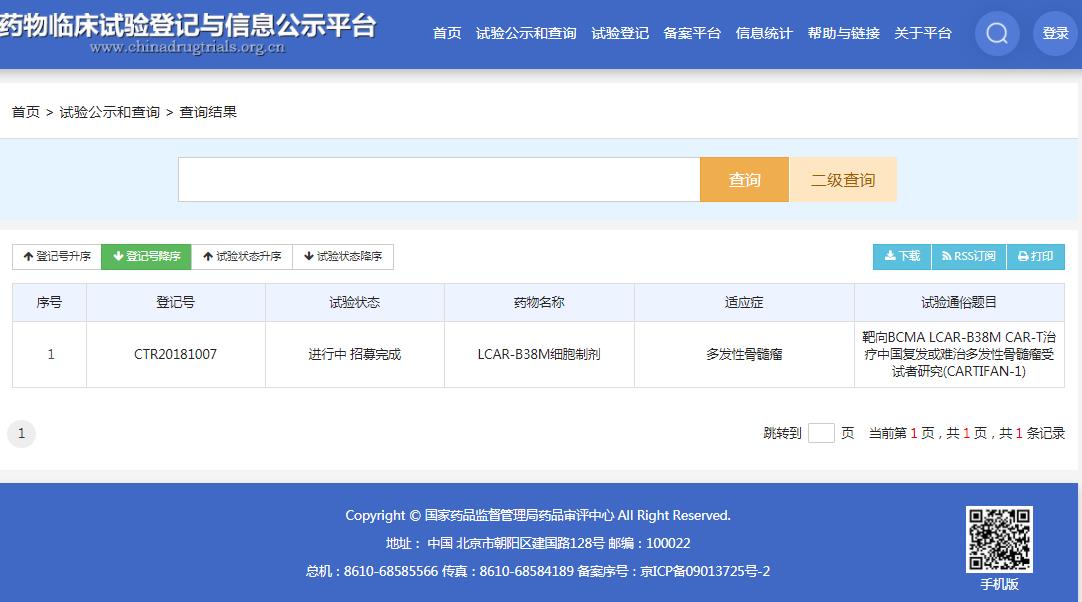
截圖來源:CDE官網
此前被納入突破性療法的傳奇生物/強生合作開發的 LCAR-B38M / JNJ4528 同樣是靶向 BCMA。該藥進展快于 CT053,目前已啟動 全球隨機 3 期臨床試驗( CARTITUDE-4)。此外,同靶點 CAR-T 產品中,BMS/藍鳥生物的 idecabtagene vicleucel (ide-cel,bb2121) 也是競爭者。
訂購需求
- *聯系人
- *聯系電話
- *咨詢品種
- 特殊備注
如緊急,請撥打
400-168-0606電話咨詢。




